カシミヤの質の評価から造血幹細胞の研究へ転進
プロテオミクスを駆使し蛋白質構造を次々解明(前編)
増田豪(熊本大学大学院 生命科学研究部 微生物薬学分野 助教)
2017.10.26

毛織物のカシミヤに含まれる蛋白質の同定・定量の研究をきっかけに、プロテオミクスの“技”を洗練させ、細胞の膜蛋白質、さらには赤芽球の蛋白質の解析に取り組んできた、熊本大学大学院生命科学研究部微生物薬学分野の増田豪氏。胎児型ヘモグロビンの発現を2つの転写因子が独自に抑制することを明らかにし、2016年の『Science』誌に論文が掲載された。現在は造血幹細胞の自己複製と分化を制御する機構の解明を進めつつ、プロテオミクスを超える新たな技術を開発し、次なる飛躍を目指している。
2016年1月15日発行の『Science』誌に、「Transcription factors LRF and BCL11A independently repress expression of fetal hemoglobin」と題した私と前田高宏先生(現・九州大学病院遺伝子・細胞療法部)の共著の論文が掲載されました。日本語にすると「2つの転写因子LRFとBCL11Aはそれぞれ独自の機構により胎児型ヘモグロビンの発現を抑制する」というタイトルになります。プロテオミクスから血液疾患という新しい研究分野に飛び込み、3年近い年月をかけた研究成果であるだけに、苦労が報われたと素直に喜びました。
胎児型βグロビンは、鎌状赤血球症の症状を軽減することが知られています。その発現を抑制する転写因子が明らかになったことで、今後、鎌状赤血球症などの病気の治療につながると期待しています。

胎児型ヘモグロビンの発現を
2つの転写因子が独自に抑制
鎌状赤血球症やβサラセミアは、成人型βグロビン遺伝子が変異することで発症します。造血幹細胞移植以外には根治的な治療法がなく、感染症や貧血によって早期に死亡する人が数多くいます。一方で、患者さんの胎児型βグロビン遺伝子プロモーター領域に特異的な遺伝子変異があると、胎児型ヘモグロビンが少し上昇し、それによって症状が軽くなることが知られています。従って、患者さんの血中の胎児型ヘモグロビンを効率良く安全に増加させる薬剤が開発されれば、予後は劇的に改善されると期待されます。
これまで転写因子のBCL11AがNuRD複合体を形成して胎児型βグロビンの発現を抑制することが報告されていました。しかし、BCL11Aを欠損させても胎児型βグロビンの発現抑制は完全には解除されず、ほかのメカニズムがあると考えられました。
私が注目したのは、マウスにおいて胚型βグロビンの発現量に関与する転写因子LRFです。LRFノックアウトマウスでは、成体からは検出されない胚型βグロビンが検出されていました。そこで、ヒトの赤芽球でLRFを欠損させることで胎児型βグロビンの発現量が変化するかどうかを検証しました。
胎児型ヘモグロビンをほとんど発現しないヒトの赤芽球細胞株(HUDEP-2細胞)を用い、LRFを欠損させた結果、胎児型βグロビンの発現量が劇的に増加することが確認され、LRFが胎児型βグロビン遺伝子の発現抑制に関与していると推測されました。
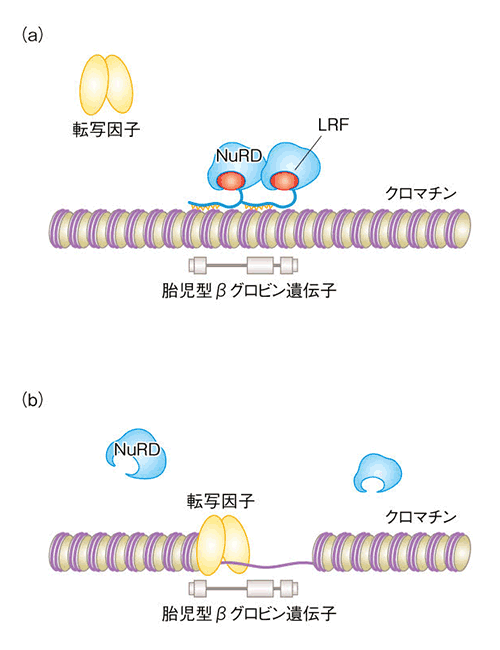
さらなる研究によって、LRFが胎児型βグロビン遺伝子とその近傍に結合することが見出され、LRFは胎児型βグロビン遺伝子に直接結合する抑制蛋白質と同定しました。さらに、転写活性の高いクロマチン構造が開く領域を調べた結果、LRF存在下では胎児型βグロビン遺伝子近傍は凝集していましたが、LRF欠損下ではクロマチン構造は開いていることが分かりました(図)。これらのことからLRFは胎児型βグロビン遺伝子の転写抑制に不可欠であると考えられます。
次に、遺伝子の発現には蛋白質複合体が関与していることが多いという事実をもとに、LRFと直接相互作用する蛋白質を調べました。その中で着目したのが、BCL11Aと相互作用することで胎児型βグロビン遺伝子の発現を抑制するとされるNuRD複合体です。ヒトの赤芽球を用いてLRFとNuRD複合体との相互作用を調べたところ、NuRD複合体の構成蛋白質のうち4つと相互作用することが分かりました。一方、LRFと結合したNuRD複合体は、BCL11Aとは相互作用しませんでした。
これらのことから、LRFおよびBCL11Aが独立して形成するNuRD複合体は胎児型βグロビン遺伝子の発現を抑制しており、かつ胎児型βグロビン遺伝子の発現の抑制機構はLRFを介した経路およびBCL11Aを介した経路によって、ほぼ完全に制御されていることが明らかになったのです。LRFとNuRD複合体が結合できないような化合物が見出されれば、胎児型βグロビンが発現し、鎌状赤血球症の予後が改善されると期待されます。
今回の研究結果は、鎌状赤血球症やβサラセミアという血液疾患に関するものですが、実は私は、血液疾患における蛋白質の研究を専門にしているわけではありません。私がプロテオミクスという技術に出合い、使い始めたのは、カシミヤという毛織物の品質の評価のためだったのです。
